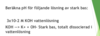Fysikalisk kemi 2 Flashcards
Vad är vattnet jonprodukt vid 25 grader?
1,01 x 10^14
Definiera en syra
En partikel som kan avge en proton H+ (protongivare)
Definiera en bas
En partikel som kan ta upp en proton H+ (protontagare)
Mot varje syra svarar en bas, vad kallas ett sådant syra-baspar?
Korresponderande syra-baspar

För att en syra skall kunna avge en proton måste en bas ta upp den samtidigt, varför?
Protonen kan ej förekomma fritt i en lösning
Vad händer vid en protolys?
Reaktion där en protonövergång sker
Ett gemensamt namn för syror och baser?
Protolyter
Vilket är de viktigaste lösningsmedlet?
Vatten
Vad är amfolyter?
Ämnen som kan fungera både som syra och som bas
Hur är förhållandet mellan pH-värdet, koncentration och H+?
pH-värdet ökar då H+ minskar, samt att en ökning av en enhet i pH ger en koncentration som blir 10 gånger mindre
I 25 grader, vid vilket ph definieras en lösning som: sur, basisk, neutral?
pH < 7.0 : sur
pH = 7.0 : neutral
pH > 7.0 : basisk
Vad är pH värdena för dessa olika kroppsvätskor: Blod, modersmjölk, galla, magsaft, magsaft (parietal sekretion), pankreassekret, tarmsekret, cerebrolspinalvätska, saliv, intracellulärvätska.
Blod: 7,4
Modersmjölk: 6,6-6,9
Galla: 7,8
Magsaft parietal sekretion: 0,87
Magsaft: 1,2-3
Pankreassekret: 7,8-8.0
Tarmsekret: 7,7
Cerebrospinalvätska: 7,4
Saliv: 6,3-6,8
Intracellulärvätska: 6,1-6,9
Vad består en pH-meter av?
Två elektroder och en högohmig voltmeter
Hur fungerar en pH-meter?
pH-elektroden känner av hur mycket H+ det finns i en lösning. Ju fler joner, desto större ström passerar genom elektroden. Strömmen visas på mätinstrumentets pH-skala
Hur kalibrerar du en pH-mätare?
De flesta pH-mätare fungerar på samma sätt, med minst 2- punktskalibrering. Kalibreringen utgår alltid från pH 7 som är neutralvärdet. Därefter väljer du själv det andra värdet pH 4 eller pH 10, beroende om du ska mäta surt eller basiskt. När mätaren accepterat kalibreringen övergår den omgående till mätning.
Vad gör mät-elektroden på pH-metern?
Mät-elektroden används för att mäta spännings-skillnaden mellan kaliumklorid (KCl) med neutralt pH 7,0 inneslutet inom ett känsligt glasmembran, och den okända vätskan som ska mätas. Mät-elektroden består av en silverklorid- (AgCl) spets nedsänkt i KCl och sen en svag HCl-lösning. Denna spänningsskillnad kan sen översättas till en pH-mätning av den okända lösningen.
Vad används referens-elektroden till
Referens-elektroden används för att fullborda kretsen och ge en känd referens-spänning för mätaren. Den består av en kvicksilverklorid- (HgCl) elektrod i KCl-lösning som ju har standardiserat neutralt pH till 7,0.
Då en syra löses i vatten, inställer sig jämvikten:

Jämviktens läge beror på?

Är det starka eller svaga syror som protolyseras fullständigt i vatten? Och hur är dess korresponderande baser?
De är de starka syrorna som protolyseras fullständigt i vatten, deras baser är så ledes svaga
Vad säger en hög syrakonstant oss?
Att syran protolyserats till 100%
När en syra protolyseras fullständigt uppkommer de då någon jämvikt mellan syran och dess joner?
nej
Åt vilket håll är jämvikten markant förskjuten för svaga syror?
jämvikten är markant förskjuten åt vänster.
Ex sådana syror är ättiksyra HAc, och salpetersyrlighet HNO2.
Svaga syror protolyseras i mindre grad än starka syror vid given temperatur och koncentration
I en 0,1 M lösning av ättiksyra, hur mycket av ättiksyramolekylen har reagerat med vattnet?
I en 0,1 M lösning av ättiksyra, har endast cirka 1 % av ättiksyramolekylen reagerat med vatten.
Hur protolyseras svaga syror i vattnet?
De protolyseras delvis
När kan protolysgraden beräknas?
När vissa molekyler förblir oprotolyserade
Hur är svaga syrors konjugerade baser?
De konjugerade baserna är svaga, och visar då en svag förmåga att avlägsna protoner från vatten
Infinner de sig en jävikt mellan den svaga syran och dess joner?
Ja
Vad säger syrakonstanten oss?
Ju högre syrakonstant desto starkare syra och motsvarande, ju lägre konstant desto svagare syra.
Protolyseras starka baser helt i vatten?
Ja
Bildar starka baser gärna en bindning med sina elektroner till en prototon?
Ja
Vad säger en stor baskonstant oss?
Att basen är stark
Vad bildar OH- (ghydroxidjonen) och är partiellt protolyserat i vatten?
Svaga baser som är molekyler eller joner
Är svaga baser dåliga eller bra proton acceptorer?
Dåliga
Hur är baskonstanten om du har en svag bas?
Den är låg
Vid en protolys av svag bas, vad förblir oprotolyserat?
Några NH3 molekyler
Vad kallas jämviktskonstanten för reaktionen mellan en bas och vatten ?
Basens protolyskonstant eller baskonstant
Nämn några starka syror
HCI, HBr, HNO3, H2SO4, HCIO3 och HCIO4
Vid fullständigt protolys av en stark syra bildas vadå?
H3O+
Vad beror pOH och pH av en stark bas på?
Molariteten hos basen
Vad krävs för att en hydroxid skall kunna fungera som en bas?
Den skall vara löslig
I en vattenlösning där svaga syror och baser partiellt protolyserats hittar vi?
En mix av joner och ojoniserade syror och baser
Varför är de just svaga syror och baser som förekommer i jämviktsreaktioner?
På grund utav att de endast partiellt är protolyserade i vattenlösningen. Vi kommer därför får en mix av joner och ojoniserade syror eller baser i lösningen
Vad är de som skiljer ett syra-bas par åt?
Endast en H+ skillnad
Visa vattnets autoprotolys

Hur är förhållandet mellan Ka Kw och Kb?
Ka x Kb = Kw
Hur är förhållandet mellan Ka och Kb?
Ju större Ka är desto mindre blir Kb. Det betyder att ju starkare syran är desto svagare är dess konjugerande bas