Nenne die Rolle des Pathologen bei einer Neoplasie
- korrekte Diagnosestellung
- Therapierelevante Veränderungen im individuellen malignen Tumor finden = personalisierte Onkologie
Welche grundliegenden Tumorformen werden unterschieden?
Dignität von Tumoren = biologisches Tumorverhalten
1. benigne = gutartig
- > verdrängendes Wachstum
- > keine Metastasen
i. d.R. chirurgisch heilbar
2. maligne = bösartig
- > infiltratives Wachstum
- > Metastasierung
potentiell lebensbedrohlich
Wie unterscheiden sich benigne und maligne Tumore in folgenden Kriterien
- Wachstum
- Proliferation
- Mitosen
- Begrenzung
- Metastasierung
- Differnzierung
- Zellatypie
- Umgebung
- Komplikationen
B = Benigne // M = Maligne
1. Wachstum:
B = eher langsam / verdrängen
M = eher schnell / invasiv-destruierend
2. Proliferation:
B = niedrig
M = hoch
3. Mitosen:
B = selten
M = zahlreich, atypisch
4. Begrenzung:
B = scharf / Kapsel
M = unscharf
5. Metastasierung:
B = keine
M = Metastasierung
6. Differenzierung:
B = hoch
M = Differenzierungsverlust
7. Zellatypie:
B = niedrig
M = hoch
8. Umgebung:
B = Kompression
M = Invasion/ Destruktion
9. Komplikation:
B = Kompression
M = Lokalrezidive, Metastasen
Systematik maligner Tumore
Was sind:
Karzinome, Sarkome, Lymphome, Keimzelltumore, Keimstrangstromatumore, maligne Melanome, Blastome
Karzinom: –> 80%
immer Epithelial, immer Maligne
Sarkome:
Mesenchymal
Lymphome / Leukämie:
Lymphatisches Gewebe / Knochenmark
Keimzelltumore:
Keimzellen
Keimstrangstromatumore:
-> Keimzellen umgebendes Stroma
maligne Melanome:
Neuro-Ektoderm
Blastome:
Embryonal unreife Zellen/ Tumore häufig im Kindesalter
Epidemiologie Tumorerkrankungen
Nenne häufigste Tumorerkrankungen bei Mann und Frau und die dazugehörigen wichtigen Letalitäten
Inzidenz Frau:
- Brustdrüse / 27%
- Darm / 17,5%
- Lunge / 6%
Letalität Frau:
- Brustdrüse / 18%
- Darm / 14%
- Lunge / 11%
Inzidenz Mann:
- Prostata / 25%
- Darm / 16%
- Lunge / 14%
Letalität Mann:
- Lunge / 26%
- Darm / 12,4%
- Prostata / 10,1%
Erkläre die TNM Klassifikation
TNM-Klassifikation
T = Tumor: Ausbreitung im ENtstehungsorgan
N = Nodus: Metastasierung in regionale Lymphknoten
M = Metastase: Fernmetastasierung
T: 1-4 –> für jeden Tumor definiert
N: 0-3 –> relevante LK für jedes Organ definiert
M: 0-1 (Metastase ja / nein)
wichtige Präfixe:
c = Klinisch
p = postoperativ (pathologisch)
r = Rezidivtumor (nach tumorfreiem Intervall)
y = nach Therapie
a = autoptisch
zusätzliche Angioinvasion:
V = Veneninvasion (V0-2) / mikroskopisch / makroskopisch
L = Lymphgefäßinvasion (L0-1)
zusätzlich Beurteilung Residualtumor:
R0 = kein Residualtumor
R1 = mikroskopisch
R2 = makroskopisch
RX = nicht beurteilbar
erkläre die Klassifikation des hier gezeigten Präparats eines Kolonkarzinom
pT3, pN1(2/16), MX, L1, V0, R0
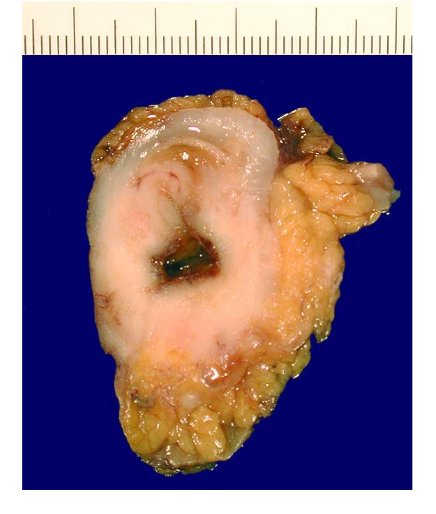
pT3 = postoperativ ausbreitung 3
pN1 = postoperativ Lymphknotenmetastase regional
MX = Metastasierung weiter nicht beurteilbar
L1 = Lymphgefäßinvasion
V0 = keine Veneninvasion
R0 = kein Residualtumor
Was bedeutet Metastasierung
Nenne die Metastasierungswege und erkläre die Bedeutung der Metastasierung
Verschleppung der Tumorerkrankung vom primären Entstehungsort an einen anderen Ort
Bedeutung:
potentiell chirurgisch beherrschbare Erkrankung wird zur
- > systemischen Erkrankung
- > systemische Therapie
Metastasierungswege:
Hämatogen
Lymphogen
Kavitär
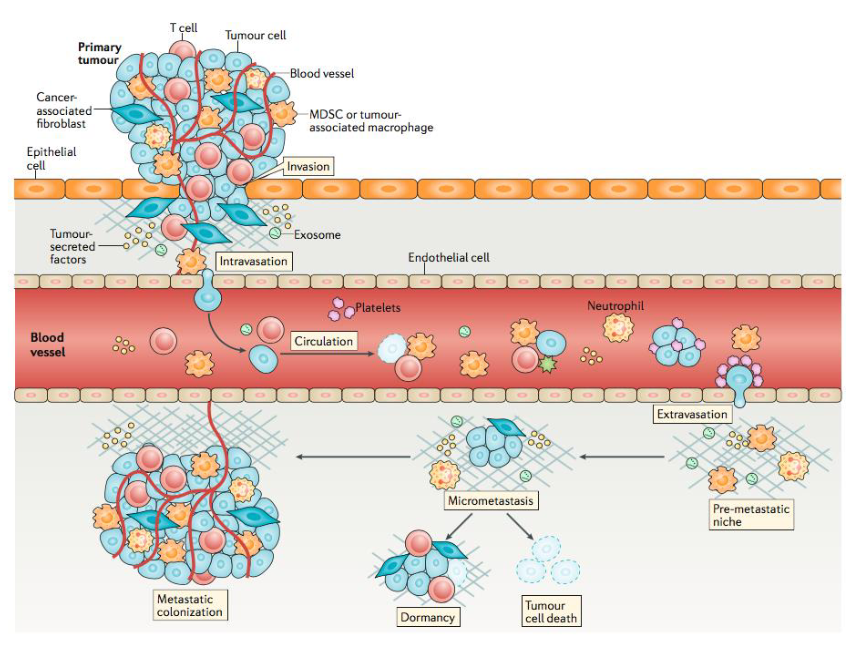
Erkläre den Vorgang der Metastasierung (beispiel Hämatogen)
maligner Tumor wächst invasiv und destruierend
- wächst in die Blutgefäße ein = Intravasation
- besteht im Blutgefäß
- wächst aus dem Blutgefäß aus = Extravasation
dann. .. mehrere Möglichkeiten
- > die metastasierten Tumorzellen benötigen im Zielorgan eine Pre-metastatische Nische!!
- > diese Nischenentstehung ist noch nicht genau verstanden aber man weiß dass schon vor der letztendlichen Metastasierung im Zielorgan diese Nische gebildet wird!
–> ein Teil der Matsatasierten Zellen “schlafen” teilweise = diese Zellen proliferieren nicht mehr und deshalb wirken hier uch viele Wirkstoffe nicht mehr die auf Zellproliferation setzen -> fangen Jahre später wieder an zu Metastasieren (bis zu 20-30 Jahre nach entstehung)
–> ein anderer Teil der Zellen fängt an zu wachsen und bildet dann nach einiger Zeit einen sichtbaren Metastatischen Tumor
Erläre wichtige Aspekte der Lymphknotenmetastasierug
Was sind Sentinel-Lymphknoten
Lymphogene Metastasierung
die Metastasierung beginnt bei einem s.g. Sentinel (Wächter) Lymphknoten
- > von da aus dann weitere nachgeschaltete regionale Lymphknoten
- > dann weiter in weitere Lymphknoten (nicht mehr regionär)
Lympknotenmetastasen sind Indikatoren für gerelle Metastasierungsfähigkeit eines Tumors
Nenne zu
Mamma-CA
Melanom
Kolon-CA
Magen-CA
die Operationsform und die Lymphknoten-Untersuchungen
Mamma-CA -> Brustdrüsenoperation
-> Lymphknoten: Axillektomie oder Sentinel-Lymphknoten
Melanom -> Hautoperation
–> Resektion der regionalen Lymphknoten oder Sentinel Lymphknoten
Kolon-CA -> partielle Colektomie
–> am Präparat enthaltene Lymphknoten
Magen-CA -> partielle Gastrektomie
–> am Präparat enthaltene Lymphknoten
Erkläre die Hämatogene Metastasierung
welche Formen werden unterschieden?
Hämatogen = Tumorinfiltration in die Blutbahn
unterschieden:
Cava-Typ
Pfortader-Typ
(je nach anatomischem Stromgebiet des Ursprungsorgans des Tumors)
Nenne die Hämatogen-Metastasierenden Organe des Cava-Typs
Niere
Zervix
Harnblase
Endometrium
Prostata
Schilddrüse
–> metastasieren in die Lunge
Nenne die hämatogen-metastasierenden Tumore des Pfortader-Typs
Magen
Kolon
Pankreas
Dünndarm
-> metastasieren in die Leber
Was ist eine kavitäre Metastasierung?
Nenne Beispiele
Kavitär = Lokale Ausbreitung nach Einbruch in eine Körperhöhle
Beispiele:
Ovarial-CA –> zu Peritonealkarzinose
Bronchus-CA –> Pleurakarzinose
Welche Karzinome führen potential zu einer Peritonealkarzinose?
Peritonealkarzinose potentiell durch:
Magen-CA
Ovarial CA
Pankreas CA
Gallenblasen CA …
Lokalisartion: Douglas meist maximal involviert!!
Welche Karzinome führen potentiell zu einer Pleurakarzinose?
durch:
Bronchus CA
Mamma CA …
Lokalisation:
ganze Pleura
DD: zu Pleuramesotheliom
Wodurch kommt es potentiell zu eienr Pericarditis carcinomatosa
durch Bronchus / Mamma / andere Karzinome die durchbrechen
Komplikationen: Perikarderguss -> Tamponade
konstriktive Kardiomyopathie
Nenne lokale Tumorkomplikationen
- Stenosen von Hohlorganen:
Bronchus, Darm, Gallenwege, andere
(am Darm beispielsweise erkennbar wo oral und aboral ist weil sich vor der Stenose der Stuhl staut und das Darmlumen erweitert wird)
- Einwacsen in Nachbarorgane:
Gefäße, Stenosen, Ulkus, etc.
- Fistelbildung
Tumorfiltration von 2 Hohlorganen:
- > Tumorzerfall
- > Lumenbildung
Beispiele:
Ösophagus-Trachea
Rektum-Vagina-Harnblase
Nenne humorale Komplikationen von Tumoren
1. Kachexie (ungewollte gewichtsabnahme)
- > Auszehrung, Kräftezerfall, Gewichtsabnahme
- > Infektionsanfällig
Pg: Tumorstoffwechselprodukte
- > kataboler Proteinumsatz
- > Mobilisierung von Fetten
- > vermehrter Energieverbrauch
- > Störung im Hugerzentrum
- TNF alpha (Kachexin)
2. Anämie
- > häufig
- > Blutverlust
- > Mangel an AS, Vitaminen
- > Hämolyse
- > Verdrängung der Myelopoese
–> paraneoplastisch
3. Paraneoplastische Syndrome
- > Krankheitszustände durch abnormale Sekretion von Produkten durch Tumor
- > oder immunologische Interaktion von Tumorproteinen mit körpereigenen Proteinen (tumorbedingte Autoimmunreaktion)
- > Hormone
- > Gerinnungsfaktoren
- > Wachstumsfaktoren
- > Antukörperbildung
Arten:
- > Endokrinopathie
- > Neurologische und muskuläre Syndrome
- > Dermatologische Störungen
- > Vaskuläre Veränderungen
- > Hämatologische Veränderungen
Paraneoplastische Syndrome
erkläre die Endokrinopathie / nenne Beispiele
Endokrinopathien:
Cushing Syndrom (ACTH und analoge Substanzen)
Hyperparathyreodismus (Parathormon)
Karzinoidsyndrom (Serotonin, Histamin)
Polyzythämie (EPO)
Hyponatriämie (ADH)
Hypoglycämie (Insulin und analoge SUbstanzen)
Beta-HCG
Nenne Tumore mit höufigen Knochenmetastasen
Prostata CA
Mamma CA
Schilddrüsen CA
Nieren CA
Bronchus CA
Histologische Klassen von Knochenmarksmetastasen:
- Osteoblastisch: Mamma oder Prostata
- Osteolytisch
Komplikationen
zu welchen Knochenmarksveränderungen kann es kommen
Vorkommen:
Hämatologische Neoplasien (Lymphome oder Leukämie)
Karzinome (sehr selten)
Komplikationen:
Anämie - extramedulläre Blutbildung
Thrombopenie
Leukopenie
Nenne zu den Gewebe jeweils den Namen der benignen und malignen Neoplasie
- Epithelien
Plattenepithel
Urothel
Drüsenepithel
- Mesenchymal:
Bindegewebe
glatte Muskulatur
quergestreifte Muskulatur
Fettgewebe
Knorpelgewebe
Knochengewebe
Blutgefäße
Lymphgefäße
Meningen
lymphatisches Gewebe
hämatopoetisches Gewebe
Epithelien:
Papillom / Plattenepithelcarzinom
Papillom / Urothelcarzinom
Adenom / Adenocarzinom
Mesenchymales Gewebe:
Fibrom / Fibrosarkom
Leiomyom / Leiomyosarkom
Rhabdomyom / Rhabdomyosarkom
Lipom / Liposarkom
Chondrom / Chrondrosarkom
Osteom / Osteosarkom
Hämangiom / Angiosarkom
Lymphangiom / Lymphangiosarkom
Meningeom / Menigeosarkom
- / Lymphom
- / Leukämie
























