Química: Ligações Químicas
V ou F?
Um átomo pode adquirir estabilidade dando, recebendo ou compartilhando elétrons.
Verdadeiro.
Química: Ligações Químicas
Podem ser de três tipos. São elas…
- Ligação iônica;
- Ligação covalente;
- Ligação metálica.
Química: Ligações Químicas
Teoria do octeto
A estabilidade de um átomo é adquirida quando o mesmo apresenta possui 8 elétrons na camada de valência, ou 2 elétrons quando possui apenas uma camada.

Química: Ligações Químicas
V ou F?
A teoria do octeto é aplicada a todos os átomos.
Falso
A teoria do octeto não é aplicada a todos os átomos (constituem exceções os metais de transição, por exemplo)
Química: Ligações Químicas
A ligação iônica também é conhecida como…
heteropolar ou eletrovalente.

Química: Ligações Químicas
Ligação iônica
Por receber essa denominação, ocorre entre…
íons (cátions e ânions).
Química: Ligações Químicas
Ligação iônica
Pode ocorrer entre quais grupos?
- Metal + ametal;
- Metal + semimetal;
- Metal + hidrogênio.
Química: Ligações Químicas
Ligações iônicas
Os metais tendem a _______ (perder/ganhar) elétrons.
Perder.
Química: Ligações Químicas
Ligações iônicas
Os ametais tendem a _______ (perder/ganhar) elétrons.
Ganhar elétrons.
Química: Ligações Químicas
Ligação iônicas
Como representar?
- Fórmula eletrônica;
- Fórmula iônica;
- Fórmula molecular.
Química: Ligações Químicas
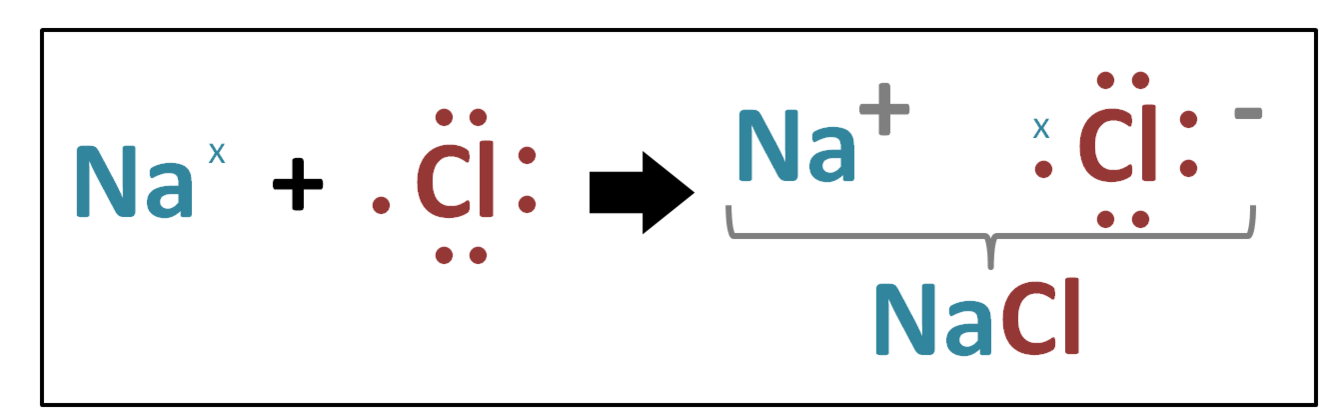
Fórmula eletrônica
Também conhecida como…
Formula de Lewis.
Química: Ligações Químicas
Fórmula eletrônica
O que exibe?
- Elementos;
- Número de átomos envolvidos;
- Elétrons da camada de valência;
- Formação de pares eletrônicos.
Química: Ligações Químicas
V ou F?
Na fórmula eletrônica os elétrons são representados por pontos ao redor do átomo.
Verdadeiro.

Química: Ligações Químicas
O cloreto de sódio (sal de cozinha) é formado por uma ligação _______ (iônica/covalente).
Ligação iônica.

Química: Ligações Químicas
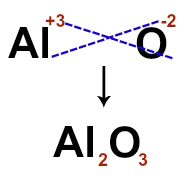
Fórmula iônica
O que designa?
Íons formados a partir da ligação e a proporção entre eles.
Química: Ligações Químicas
Na representação por meio de fórmulas Escreve-se sempre primeiro o ________ (ânion/cátion) e depois o _________(ânion/cátion).
Primeiro o cátion e depois o ânion.

Química: Ligações Químicas
Fórmula molecular
Também conhecida como…
Fórmula bruta.
Química: Ligações Químicas
Fórmula molecular
O que indica?
Indica apenas número de átomos de cada elemento em uma molécula.

Química: Ligações Químicas
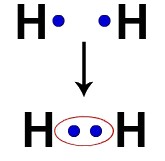
Ligação covalente
Como se dá?
Por meio do compartilhamento de elétrons.
Química: Ligações Químicas
V ou F?
Na ligação covalente não existe a formação de íons.
Verdadeiro.
Química: Ligações Químicas
V ou F?
Na ligação covalente não existe a mudança permanente de elétrons.
Verdadeiro.
Química: Ligações Químicas
Os compostos formados por meio de ligações covalentes são eletricamente __________ (positivos/neutros).
Neutros.
Química: Ligações Químicas
Ligação covalente
Pode ocorrer entre quais grupos?
Hidrogênio, ametais ou semimetais + Hidrogênio, ametais ou semimetais.
Química: Ligações Químicas
A molécula de água tem origem a partir de uma ligação _______ (iônica/covalente).
Covalente.












