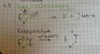OC1 Flashcards
Radikal
- Verbindung mit Ungepaarten Elektronen reaktive
- Zwischenstufe
- stabiele: NO, NO2
- Erzeugung: Bindungsspaltung (Homolyse) Aus Radikalen (Kettenreaktion) Singel elektron transfer
BDE
H-H 436 kJ/mol
C-H 400-430 kJ/mol
C-C 350 kJ/mol
Hammond Postulat
Halogenalkane
Siede- und Schmelzpunkt höher als Alkane
Ursache : polare Bindungen(Dipol)
Reaktion: Sn und E
Nucleophile
Neutrale Verbindungen mit freiem Elektronenpaar oder Anion
Bsp.: OH-, OR-, Br-, NH3, H2O, Cl-
Nucleophile Substitutuion SN
SN1 oder SN2
- abhängig von Substrat
- abhängig vom Lösungsmittel
- abhängig von der Abgangsgruppe
- abhängig von der Natur des Nucleophils
Nucleophil reagiert mit Elektrophil
hart?
Weich?
HSAB-Konzept?
hart
Ladungen ziehen sich an (Reaktion ist Ladungsgetrieben), keine allg. gültige “Nucleophilie” Nucleophil ist u.a. abhängig vom Elektrophil
weich
Gute Überlappung von Orbitalen (Reaktion ist Orbitalgetrieben)
HSAB
hart reagiert mit hart
weich reagiert mit weich
ambidente Nucleophile
Bildung von C-O-Bindungen
Lsg.:Sulfonate
Eliminierungsreaktion
Konkurrenz zu SN
SN→ gutes Nucleophil, sterisch wenig Anspruchsvoll
E→ starke Base, sterisch wenig anspruchsvoll bei hoher Temperatur
E2 Konzertiert
C-H und C-X liegen in einer Ebene 180° (0° Ausnahme thermische Syn Elemenierung)
Hofman oder Saytzer?
Thermische Syn-Eliminierung
Alkene
Stabilität von Alkenen
Je höher Substituiert desto güstiger
Alkylreste schieben Elektronen duch Hyperkonjugation ins π*-Orbital
Cis-Trans
Elektrophile Addition
an unsymmetrischen Alkenen
stereokonvergent
Die Stereochemie bleibt erhalten
Moleküle mit mehreren Doppelbindungen
Diels-Alder-Reaktion
thermisch erlaubt?
2+2 Cycloaddition
Photochemisch erlaubt?
Endo und Exo
bei Diels-Alder-Reaktion
normaler Elektronenbedarf einer Diels Alder Reaktion
Dien ist Elektronen-Donor HOMO e- reich →schneller
Dienophil ist Elektronen-Akzeptor LUMO e- arm→ schneller
Ausnahme: Sehr Elektronenarmes Dien, sehr Elektronenreiches Dienophil ⇒ Diels Alder Reaktion mit inversem Elektronrnbedarf
Mesomere Effekte
Regioselektivität von Diels-Alder-Reaktionen
2+1 Cycloaddition
Cheletrope Reaktion
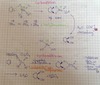
Herstellung von Dichlorcarben
Singulett und Triplett Carben
Kriterien für Aromatizität