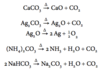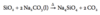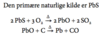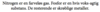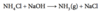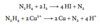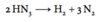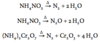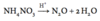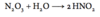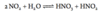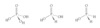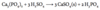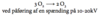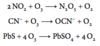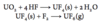13-Ugers periode Flashcards
Hvilken type bindinger danner grundstofferne i 5. hovedgruppe?
Nitrogen og fosfor laver covalente bindinger. Arsen laver netværk-covalente bindinger. Antimon og bismuth laver metalliske bindinger.
Hvilken type bindinger danner grundstofferne i 2. periode?

Hvilke type bindinger danner grundstofferne i 3. periode?

Hvilken bindingstype er der tale om i de højeste fluorider af grundstofferne i 2. periode?
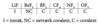
Hvilken bindingstype er der tale om i de højeste fluorider af grundstofferne i 3. periode?

Hvilken bindingstype er der tale om i de højeste oxider af grundstofferne i 2. periode?

Hvilken bindingstype er der tale om i de højeste oxider af grundstofferne i 3. periode?

Hvilken bindingstype er der tale om i hydriderne af grundstofferne i 2. periode?
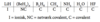
Hvilken bindingstype er der tale om i hydriderne af grundstofferne i 3. periode?

Angiv syre/base egenskaberne af de højeste oxider af grundstofferne i 3. periode

Angiv syre/base egenskaberne af de højeste oxider af grundstofferne i 5. hovedgruppe

Hvorledes kan H2 fremstilles industrielt og i laboratoriet?

Stiger eller falder reaktiviteten mellem H2 og halogenerne ned gennem 7. hovedgruppe?
Reaktiviteten mellem dihydrogen og halogenerne falder ned gennem 7. hovedgruppe.
Beskriv hvordan H2 kan anvendes som reduktionsmiddel

Hvorledes kan hydriderne af grundstofferne i det periodiske system karakteriseres som henholdsvis ioniske, kovalente eller metalliske?
Hydriderne af grundstofferne i 1. og 2. hovedgruppe kan karakteriseres som ioniske.
Hydriderne af overgangsmetallerne kan karakteriseres som metalliske.
Hydriderne af grundstofferne i 3. til 7. hovedgruppe kan karakteriseres som covalente.
Begrund hvorfor vands og flussyres kogepunkt er væsentligt højere end forventet
Intermolekylære hydrogenbindinger.


Beskriv henholdsvis lithiums reaktion med atmosfæren (oxygen og kuldioxid) samt alkalimetallernes reaktion med vand

Forklar hvorfor Li+ er exceptionel god til at koordinere vand
Li+ har godt nok kun én positiv ladning. Til gengæld er Van der Walls radius af ionen relativt lille hvilket fører til en relativt høj ladningstæthed (ladning pr. volumen). Det er ladningstætheden der afgører ionens evne til at koordinere
vand.

Opskriv alkalimetallernes flammefarver

Hvilken sammenhæng er der mellem opløseligheden af et salt, kationens radius og anionens radius?

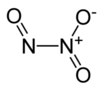
Opskriv reaktionen mellem nitrogen og et alkalimetal der har en rød flammefarve og høj ladningstæthed. Opskriv da produktets reaktion med vand.
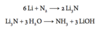
Beskriv med ord og reaktionsskema hvorledes lithium indgår i genopladelige Lithium-Ion batterier

Beskriv med reaktionsskema hvorledes lithium indgår i ikke-genopladelige batterier

Opskriv hvordan titanium fremstilles industrielt
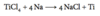
Opskriv hvordan natrium og kalium fremstilles industrielt

Opskriv hvordan natriumhydroxid fremstilles industrielt
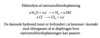
Opskriv oxiderne af alkalimetallerne samt deres reaktion med vand

Beskriv med reaktionsligninger hvorledes KO2 kan bruges til at oplagre kuldioxid
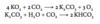
Er dioxid(2-)ionen para- eller diamagnetisk? Begrund med MO teori.

Er dioxid(1-)ionen para- eller diamagnetisk? Begrund med MO teori.

Opskriv reaktionen mellem aluminium metal og hydroxidionen

Hvad sker der med en natriumhydroxidopløsning uden låg?

Salte af alkalimetalionerne samt ammoniumionen er normalt letopløselige. Som de eneste er alkalimetalionerne f.eks. letopløselige som carbonater. Opskriv reaktioner hvorved Na+, K+ og NH4+ kan bundfældes

Beskriv med reaktionsskemaer hvorledes natriumbicarbonat anvendes i bagepulver
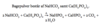
Hvad sker der med natriumbicarbonat når det opvarmes?

Beskriv med ord og reaktionsskema hvad der sker når et alkalimetal, i dette tilfælde natrium, opløses i ammoniak

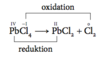
Hvordan findes kaliumchlorid i naturen og hvordan udvindes det?

Fra hvilket mineral og hvordan udvindes Na2CO3?

Beskriv hvorledes Na2CO3 kan fremstilles ud fra Solvay processen

Beskriv med reaktionsskema hvorledes Na2CO3 anvendes i produktionen af glas.

Begrund at magnesium(II) har en mindre ionradius end natrium(I)

Opskriv reaktionen mellem en (for det meste) intert gas og magnesium metal

Angiv hvilke af jordalkalimetallerne der er
opløselige med CO32–, PO3–, SO42– og OH–

Vis med reaktionsskema at berylliumoxid er amfotert

Begrund hvorfor beryllium har tendens til at danne covalente forbindelser

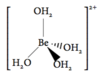
Optegn strukturen af [Be(OH2)4]2+
Hvordan findes magnesium i naturen?

Opskriv reaktion for forbrænding af magnesium metal med oxygen henholdsvis carbondioxid

Beskriv den industrielle fremstilling af magnesium

Hvad sker der når CaCO3 opvarmes?

Opskriv hovedkomponenterne i klinker samt reaktionen hvorved cement hærder
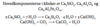
Opskriv den kemiske formel for gips og for det tilsvarende hemihydrat

Opskriv reaktionen for dannelse af calciumcarbid

Opskriv calciumcarbids reaktion med vand henholdsvis nitrogen

Opskriv reaktionen for fremstilling af bor

Opskriv den kemiske formel for de to mest almindelige salte som bor findes i i naturen

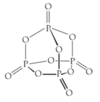
Tegn strukturen af borationen i borax

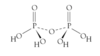
Tegn strukturen af peroxoborationen

Opskriv reaktionen for fremstilling af peroxoborationen

Opskriv reaktionen for fremstilling af borcarbid samt reaktionen for fremstilling af titaniumborid
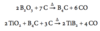
Tegn strukturen af diboran

Tegn strukturen af pentaboran(9)
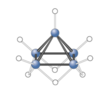
Tegn strukturen af tetraboran(10)

Beskriv fremstillingen af diboran ved hjælp af et reaktionsskema

Beskriv fremstillingen af tetraboran og pentaboran med reaktionsskemaer
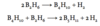
Opskriv diborans reaktion med oxygen og vand

Opskriv reaktionen for fremstilling af natriumborhydrid
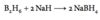
Aluminium metal er amfotert. Opskriv dets reaktion med syre henholdsvis base

Aluminium(III) i vandig opløsning er en svag syre på linje med eddikesyre. Opskriv reaktionen med vand

Beskriv den industrielle fremstilling af aluminium metal med reaktionsskemaer